- 网站首页
- 学校概况
学校简介校园风光校园视频学校发展领导之窗组织机构校史沿革规章制度
- 校园动态
校园新闻公示公告招生招聘周程安排
- 教学科研
科研动向课题研究课程设置队伍建设课例展示资源下载教学视频
- 教务管理
成绩查询教务快讯资源下载
- 德育空间
专题教育德育队伍德育活动学子风采德育课程德育在线心灵驿站爱国主义班主任信息资源库
- 体艺之窗
- 党政建设
党员风采支部建设党的群众路线教育实践活动政策文件
- 工会工作
法律法规调研文章工会要闻
- 校报校刊
- 附属幼儿园
幼儿园动态领导机构幼儿园简介
- 职称专题
- 团委
资助信息学生会社团联合会一般新闻
- 名师榜
龙湾校区龙岗校区
- 名师工作
语文工作坊梁小金工作室何萍工作室
《乙酸》教学设计
《乙酸》教学设计
一、教学目标
(一)知识与技能
1.了解乙酸的分子式和结构式,理解羧基的结构特点;
2.理解酯化反应的概念;掌握乙酸的酸性和酯化反应等化学性质;
3.能够初步熟悉乙酸的酯化反应实验的有关操作;
(二)过程与方法
1.通过展示乙酸分子的球棍模型及实物,进一步认识乙酸的分子结构及其物理性质;
2.采用复习回忆法及实验验证法学习乙酸的酸性;
3.利用实验探究﹑设疑引导学生学习乙酸的酯化反应,明确酯化反应的实质;
(三)情感﹑态度与价值观
1.培养学生的观察能力,分析归纳思维能力;
2.能够通过乙酸用途等的学习,认识化学与生产生活的密切联系,从而激发学习化学的兴趣,提高学习化学的积极性;
二、教学重点
1.乙酸的酸性
2.乙酸的酯化反应
三﹑教学难点
乙酸酯化反应的实质。
四﹑教学用具
乙酸分子的球棍模型,多媒体设备;
冰醋酸,乙酸溶液,无水乙醇,浓硫酸,饱和碳酸钠溶液,NaOH溶液,镁条,酚酞;
试管,烧杯,铁架台,酒精灯,胶头滴管,带胶塞玻璃导管。
五、教学过程
[引入] 上节课我们学习乙醇的结构和一些重要的性质,知道它是酒的主要成分,那你又是否知道:为什么酒的年份越长味道就越香?厨师烧鱼时加醋并加点酒,鱼的味道就变得无腥﹑鲜美?通过本节课的学习我们就能够知道其中的奥妙。
[板书] 生活中两种常见的有机物——乙酸
[讲述] 俗话说:“百姓出门七件事:柴、米、油、盐、酱、醋、茶”其中说到的醋的主要成分就是乙酸,所以乙酸又叫醋酸。下面我们就来学习乙酸的结构和性质。
[展示] 无水乙酸样品,让学生观察并总结乙酸的物理性质(颜色、状态和气味)。
[板书](一)、物理性质
1.无色有强烈刺激性气味的液体
2.易溶于水乙醇等溶剂
3.沸点:117.9℃ 熔点:16.6℃
[讲述] 当温度低于16.6℃时无水乙酸易凝结成冰一样的晶体,所以无水乙酸又称为冰醋酸。
[过渡] 刚才我们已经了解了乙酸的一些外观特征,那么乙酸分子的内部结构又是怎么样的呢?我们来看看乙酸分子的结构模型。
[展示] 乙酸分子的球棍模型,让学生总结乙酸的化学式、结构式和结构简式。
[板书] (二)、分子组成与结构
化学式:C2H4O2
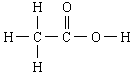
结构式:
结构简式:CH3COOH
官能团:羧基 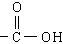 (—COOH)
(—COOH)
[讲述]乙酸可以看作是甲基和羧基组成的。
[过渡] 那么接下来我们通过几个小实验来研究一下乙酸有哪些化学性质。
[板书] (三)、化学性质
[师]根据初中已学知识,大家说说乙酸有什么性质?
[生]弱酸性
[师]根据下列药品,设计实验证明乙酸的确有酸性
药品:镁条、NaOH溶液、Na2CO3粉末、乙酸溶液、酚酞
[实验一] 乙酸与镁的反应
实验步骤:向一支盛有少量乙酸的试管里加入一小段镁条,观察现象。
实验现象:有气泡产生
实验结论:乙酸能跟活泼金属作用,具有酸性。
化学反应方程式:2CH3COOH + Mg == Mg(CH3COO)2+H2↑
[实验二] 乙酸与碳酸钠的反应
实验步骤:向一盛有少量碳酸钠粉末的试管里,加入约3mL乙酸溶液,观察现象。
实验现象:试管里有无色、无味的气泡生成
实验结论:乙酸具有酸性,且酸性比碳酸的酸性强。
相关化学反应方程式:2CH3COOH + Na2CO3 = 2CH3COONa + CO2↑+ H2O
[实验三]乙酸和氢氧化钠反应
实验步骤:先取氢氧化钠溶液于试管中,加入一滴酚酞,再逐滴加入乙酸
实验现象:红色褪去
实验结论:乙酸具有酸性
化学方程式:CH3COOH + NaOH = CH3COONa +H2O
[归纳] 通过前面几个小实验可以证明乙酸具有酸的通性:能与活泼金属、碱、盐等物质发生反应。乙酸的酸性比硫酸、盐酸等的酸性弱,但比碳酸的酸性强。
[观看“除去水垢”漫画,说出其中的道理。]
[投影]乙酸除去水垢的原理:
2CH3COOH + CaCO3 = (CH3COO)2 Ca +H2O+CO2↑
[板书] 1﹑乙酸是一种有机弱酸,具有酸的通性。
酸性强弱:H2SO4 > CH3COOH > H2CO3
[过渡] 乙酸除了具有酸的通性外,还有什么其他化学性质呢?
[演示实验] 乙酸与乙醇的反应
实验步骤:在试管里先加入3mL无水乙醇,然后一边摇动一边慢慢地加入2mL浓硫酸和2mL无水乙酸。然后用酒精灯小心均匀地加热试管3~5min。同时将导管通到装有饱和碳酸钠溶液的试管中,观察现象,注意产物的气味。
实验现象:有不溶于水,具有果香味的无色透明油状液体生成
|
|
化学反应方程式:CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O
[讲述] 通过实验得出:乙酸与乙醇在有浓硫酸存在并加热的条件可以发生反应,实验中生成的有果香味的无色透明油状液体叫乙酸乙酯。像这种酸跟醇作用生成酯和水的反应叫酯化反应。乙酸与乙醇的酯化反应是可逆的。
[板书] 2﹑酯化反应:酸跟醇作用生成酯和水的反应叫酯化反应。
[讨论]
- 不加热反应能够发生么?加热的目的是什么?(提高反应速率;使生成的乙酸乙酯挥发,有利于收集乙酸乙酯。)
2.浓硫酸的作用是什么?(催化剂和脱水剂、吸水剂)
3、为何用饱和碳酸钠溶液来吸收乙酸乙酯? (a.吸收挥发出来的乙酸和乙醇;b.使乙酸乙酯和碳酸钠溶液分层)
4.长导管有何作用?(导气和冷凝)导管为何不能伸入饱和碳酸钠溶液中?(防止倒吸)
5.在酯化反应中乙酸和乙醇有几种可能的断键方式?如何确定实际发生的是哪种断键方式?
[投影]两种可能的断键情况
[动画演示]利用同位素原子示踪法验证酯化反应的实质
[板书] 酯化反应的实质:酸脱羟基、醇脱氢(羟基上的)
[过渡]性质决定用途,乙酸具有酸性,能够发生酯化反应,决定了它具有以下用途。
[板书] ( 四)乙酸的重要用途
乙酸是一种重要的有机化工原料。可用于生产醋酸纤维、合成纤维、喷漆溶剂、香料、染料、医药以及农药等。同时,乙酸是食醋的重要成分,也可用于杀菌消毒。
[随堂练习]
[课后思考题] 以乙烯和水为主要原料如何制得乙酸乙酯?试写出相关化学反应方程式!
六.板书设计:
乙酸
(一)、物理性质
(二)、分子组成与结构
化学式:C2H4O2
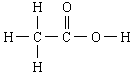
结构式:
结构简式:CH3COOH
官能团:羧基 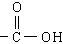 (—COOH)
(—COOH)
(三)、化学性质
1﹑乙酸是一种有机弱酸,具有酸的通性。
酸性强弱:H2SO4 > CH3COOH > H2CO3
2﹑酯化反应:
 CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O
CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O
酸跟醇作用生成酯和水的反应叫酯化反应。
酯化反应的实质:酸脱羟基、醇脱氢(羟基上的)
( 四)乙酸的重要用途
- 相关信息
- 没有相关内容
 《卤代烃》教学设计[ 02-01 ]
《卤代烃》教学设计[ 02-01 ] 高考一轮复习 《氯及其化合物》[ 02-01 ]
高考一轮复习 《氯及其化合物》[ 02-01 ]


