- 网站首页
- 学校概况
学校简介校园风光校园视频学校发展领导之窗组织机构校史沿革规章制度
- 校园动态
校园新闻公示公告招生招聘周程安排
- 教学科研
科研动向课题研究课程设置队伍建设课例展示资源下载教学视频
- 教务管理
成绩查询教务快讯资源下载
- 德育空间
专题教育德育队伍德育活动学子风采德育课程德育在线心灵驿站爱国主义班主任信息资源库
- 体艺之窗
- 党政建设
党员风采支部建设党的群众路线教育实践活动政策文件
- 工会工作
法律法规调研文章工会要闻
- 校报校刊
- 附属幼儿园
幼儿园动态领导机构幼儿园简介
- 职称专题
- 团委
资助信息学生会社团联合会一般新闻
- 名师榜
龙湾校区龙岗校区
- 名师工作
语文工作坊梁小金工作室何萍工作室
高三化学一轮复习学案设计《 原子结构》
高三化学一轮复习学案设计《 原子结构》
梁家梅
【高考考察】
1、依据原子结构进行相关推断
2、原子组成的表示方法及同位素的判断
3、原子核外电子排布知识应用于元素的判断
【学习目标】
1、知识目标:掌握基本概念,熟练运用原子结构等基础知识进行推断。
2、学会运用比较等基本方法,加深对概念的理解,并实践于题目。
【教学方法】 问题探究、比较法 教具 黑板、多媒体
【学习过程】
原子结构
一、原子的构成
【思考1】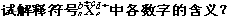
【思考2】有关数量关系
1、原子中:质子数=
2、质量数=
【思考3】填表
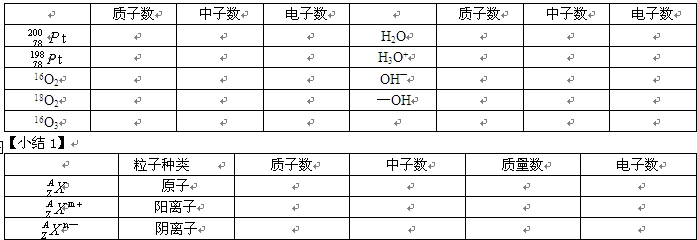
【思考4】aAm+和bBn—核外电子结构相同,则a值是( )
A、b+n+m B、b+n-m C、b-n-m D、b-n+m
【思考5】18g 2H2O中所含的质子数为 。
【小结2】
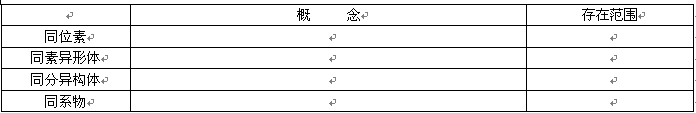
【思考6】判断下列物质间的关系
1、CH3COOH与HCOOCH3 2、红磷和白磷
3、乙烯与1-丁烯 4、 与 5、1H2O与2H2O
【思考7】(2010山东)下列说法正确的是( )
A、16O2与18O2互为同分异构体 B、16O与18O核外电子排布方式不同
C、通过化学变化可以实现16O与18O间的相互转化
D、标准状况下,1.12L16O2和1.12L18O2均含0.1NA个氧原子
【思考8】(2013大纲全国)下列关于同温同压下的两种气体12C18O和14N2的判断正确的是( )
A、体积相等时密度相等 B、原子数相等时具有的中子数相等
C、体积相等时具有的电子数相等 D、质量相等时具有的质子数相等
二、原子核外电子排布
1、电子层的划分

2、排布规律
(1)电子一般总是首先排在能量 的电子层里,即最先排在 ,当 排满后,再排 ,依次类推。
(2)每层最多容纳的电子数为 (n代表电子层数)。
(3)最外层电子数不超过 个(K层为最外层时,最多不超过 个),次外层不超过 个。
【思考9】写出符合下列条件的元素符号及对应原子序数(1-18号元素)
1、最外层电子数是次外层电子数2倍的原子 ;
2、M层电子数是L层电子数的一半的原子 ;
3、次外层电子数是最外层电子数的1/4的原子 ;
4、最外层电子数是电子层数2倍的原子 ;
5、内层电子总数是最外层电子数2倍的原子 。
【思考10】(2012全国)元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于负二价硫离子的半径。X元素为( )
Al B、P C、Ar D、K
【思考11】《优化设计》演练巩固提升5
有V、W、X、Y、Z5种元素,它们的核电荷数依次增大,且都小于20。其中:X、Z是金属元素;V和Z元素原子的最外层都只是一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此推知(填元素符号):V是 ;W是 ;X是 ;Y是 ;Z是 ;由这些元素组成的一种结晶水合物的化学式 ;俗称 。
课后练习:
《优化设计》P41有关练习
学习感悟:
- 相关信息
- 没有相关内容
 化学一轮复习教案 《化学平衡》[ 02-01 ]
化学一轮复习教案 《化学平衡》[ 02-01 ] 《气体摩尔体积》课件[ 02-01 ]
《气体摩尔体积》课件[ 02-01 ]


